Τι είναι οι ηλεκτρολύτες και οι μη ηλεκτρολύτες;Παραδείγματα και Διαφορές
2026-04-29
184
Κατάλογος
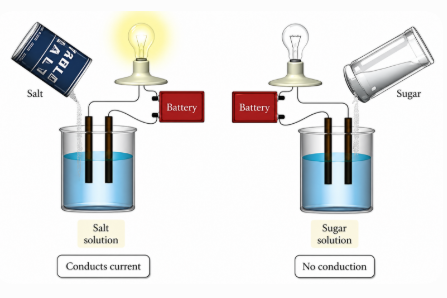
Ηλεκτρολύτες: Ιδιότητες και Συμπεριφορά
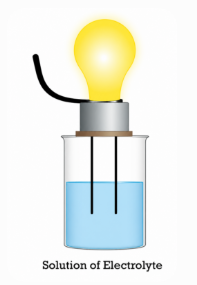
Σχήμα 2. Ηλεκτρική αγωγιμότητα ενός διαλύματος ηλεκτρολυτών
Οι ηλεκτρολύτες είναι ουσίες που διαλύονται στο νερό και παράγουν ιόντα, καθιστώντας τα διαλύματά τους ηλεκτρικά αγώγιμα και χημικά ενεργά.
1. Σχηματισμός και διάσπαση ιόντων
Όταν οι ηλεκτρολύτες διαλύονται, χωρίζονται σε κατιόντα και ανιόντα.Ο βαθμός διαχωρισμού καθορίζει τη δύναμή τους:
• Ισχυροί ηλεκτρολύτες διασπώνται πλήρως, παράγοντας πολλά ιόντα
• Αδύναμοι ηλεκτρολύτες μερικώς διασπώνται, παράγοντας λιγότερα ιόντα
Αυτό επηρεάζει τόσο την αγωγιμότητα όσο και την αντιδραστικότητα.
Παράδειγμα
Στο ανθρώπινο σώμα, τα επίπεδα ηλεκτρολυτών επηρεάζουν τα νευρικά σήματα και τον καρδιακό ρυθμό.Στις μπαταρίες, η αποτελεσματική κίνηση ιόντων βελτιώνει τη μεταφορά ενέργειας.
2. Ηλεκτρική αγωγιμότητα
Οι ηλεκτρολύτες φέρουν ηλεκτρισμό επειδή τα ιόντα μεταφέρουν φορτίο.Η κίνηση των ιόντων δημιουργεί ηλεκτρικό ρεύμα και η αγωγιμότητα αυξάνεται με τον αριθμό των ιόντων που υπάρχουν.
Παράδειγμα
Το θαλασσινό νερό μεταφέρει καλά τον ηλεκτρισμό λόγω της υψηλής συγκέντρωσης ιόντων, ενώ το καθαρό νερό έχει πολύ χαμηλή αγωγιμότητα.Τα διαλύματα ηλεκτρολυτών χρησιμοποιούνται επίσης στην ηλεκτρολυτική επίστρωση για την επικάλυψη μετάλλων.
3. Χημική αντιδραστικότητα
Οι ηλεκτρολύτες αντιδρούν στο διάλυμα επειδή τα ιόντα μπορούν εύκολα να αλληλεπιδράσουν.Αυτό επιτρέπει διαδικασίες όπως:
• Αντιδράσεις καθίζησης
• Οξεοβασική εξουδετέρωση
• Αντιδράσεις οξειδοαναγωγής
Παράδειγμα
Η ανάμειξη νιτρικού αργύρου και χλωριούχου νατρίου σχηματίζει ένα λευκό ίζημα χλωριούχου αργύρου.Αυτός ο τύπος αντίδρασης χρησιμοποιείται στην επεξεργασία και ανάλυση νερού.
4. Φύση και Σύνθεση
Οι ηλεκτρολύτες είναι συνήθως:
• Άλατα (π.χ. χλωριούχο νάτριο)
• Οξέα (π.χ. υδροχλωρικό οξύ)
• Βάσεις (π.χ. υδροξείδιο του νατρίου)
Είναι συνήθως ιοντικά ή έντονα πολικά, επιτρέποντας στο νερό να τα χωρίσει σε ιόντα.
5. Διαλυτότητα και απόδοση
Για αποτελεσματική απόδοση, οι ηλεκτρολύτες πρέπει να διαλύονται καλά και να παράγουν πολλά ιόντα.
Περιορισμός
Ορισμένες ουσίες διασπώνται αλλά έχουν χαμηλή διαλυτότητα.Για παράδειγμα, ο χλωριούχος άργυρος σχηματίζει ιόντα αλλά διαλύεται πολύ λίγο, επομένως έχει χαμηλή αγωγιμότητα.
Μη ηλεκτρολύτες: Ιδιότητες και Συμπεριφορά
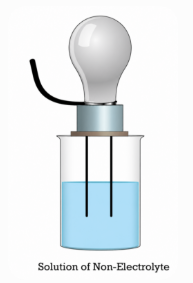
Σχήμα 3. Διάλυμα μη ηλεκτρολυτών δεν μεταφέρει ηλεκτρισμό
Οι μη ηλεκτρολύτες διαφέρουν επειδή δεν σχηματίζουν ιόντα στο διάλυμα.Αυτό περιορίζει την αγωγιμότητα και την ιοντική αντιδραστικότητα τους.
1. Χωρίς σχηματισμό ιόντων
Όταν οι μη ηλεκτρολύτες διαλύονται, παραμένουν ως ουδέτερα μόρια.Δεν παράγονται φορτισμένα σωματίδια.
2. Έλλειψη ηλεκτρικής αγωγιμότητας
Δεδομένου ότι δεν σχηματίζονται ιόντα, οι μη ηλεκτρολύτες δεν μεταφέρουν ηλεκτρισμό.Ακόμη και με εφαρμοζόμενη τάση, δεν ρέει ρεύμα.
Παράδειγμα
Η ζάχαρη που διαλύεται στο νερό δεν μεταφέρει ηλεκτρισμό, ενώ το αλμυρό.Η διαφορά είναι ο σχηματισμός ιόντων, όχι η διαλυτότητα.
3. Περιορισμένη χημική αντιδραστικότητα
Οι μη ηλεκτρολύτες δεν συμμετέχουν στις ιοντικές αντιδράσεις.Αντίθετα, εμπλέκονται σε:
• Μοριακές αντιδράσεις
• Βιοχημικές διεργασίες
• Αντιδράσεις που σχετίζονται με την ενέργεια
Παράδειγμα
Η γλυκόζη δεν σχηματίζει ιόντα αλλά είναι σημαντική για την παραγωγή ενέργειας στα κύτταρα.
4.Φύση και Σύνθεση
Οι περισσότεροι μη ηλεκτρολύτες είναι ομοιοπολικές ενώσεις, συχνά οργανικές, όπως:
• Ζάχαρα
• Αλκοόλ
• Ουρία
Διαλύονται χωρίς να διασπώνται σε ιόντα.
5. Διαλυτότητα χωρίς αγωγιμότητα
Πολλοί μη ηλεκτρολύτες διαλύονται στο νερό αλλά παραμένουν ουδέτεροι.Αυτό δείχνει ότι η διαλυτότητα από μόνη της δεν εγγυάται την αγωγιμότητα.
Ηλεκτρολύτες vs Μη ηλεκτρολύτες
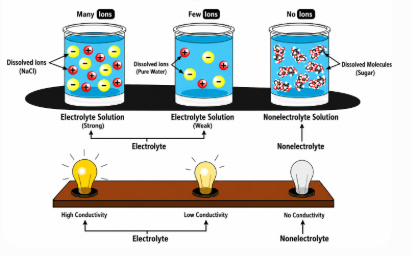
Σχήμα 4. Σύγκριση ηλεκτρολυτών έναντι μη ηλεκτρολυτών
|
Βάση |
Ηλεκτρολύτες |
Μη ηλεκτρολύτες |
|
Σχηματισμός Ιόντων |
Σχηματίζει ιόντα |
Χωρίς σχηματισμό ιόντων |
|
Αγωγιμότητα
|
Διεξαγωγή ηλεκτρικής ενέργειας |
Μην συμπεριφέρεστε |
|
Σωματίδια σε Διάλυμα |
Ιόντα |
Ουδέτερα μόρια |
|
Τύπος ομολόγου |
Ιονικό ή πολικό ομοιοπολικό |
Ομοιοπολική |
|
Αντιδραστικότητα |
Ιονικές αντιδράσεις |
Μοριακές αντιδράσεις |
|
Παραδείγματα |
NaCl, HCl, ΚΟΗ |
Γλυκόζη, αιθανόλη |
Πρακτικές χρήσεις και σημασία
Η κατανόηση αυτών των ουσιών έχει πρακτικές εφαρμογές.
Υγεία και Ιατρική
Οι ηλεκτρολύτες ρυθμίζουν την ενυδάτωση, τα νευρικά ερεθίσματα, τη σύσπαση των μυών και τον καρδιακό ρυθμό.Όταν τα επίπεδα ηλεκτρολυτών είναι ανισορροπημένα, μπορεί να οδηγήσει σε κόπωση, κράμπες ή ακόμα και σοβαρά προβλήματα υγείας.
Ενέργεια και Τεχνολογία
Οι ηλεκτρολύτες χρησιμοποιούνται σε μπαταρίες, κυψέλες καυσίμου και άλλες ηλεκτροχημικές συσκευές.Για παράδειγμα, οι μπαταρίες ιόντων λιθίου βασίζονται στην κίνηση των ιόντων για την παραγωγή και αποθήκευση ενέργειας, επιτρέποντάς τους να τροφοδοτούν αποτελεσματικά τις συσκευές.
Χημεία και Βιομηχανία
• Οι ηλεκτρολύτες ενεργοποιούν:
Οι ηλεκτρολύτες χρησιμοποιούνται σε χημικές αντιδράσεις σε διάλυμα, εξαγωγή και καθαρισμό μετάλλων και διεργασίες ηλεκτρόλυσης.
• Οι μη ηλεκτρολύτες είναι σημαντικοί σε:
Οι μη ηλεκτρολύτες χρησιμοποιούνται σε τρόφιμα και φαρμακευτικά προϊόντα, βοηθούν στη διατήρηση της χημικής σταθερότητας και υποστηρίζουν ελεγχόμενες αντιδράσεις.
Συνήθεις παρανοήσεις για τους ηλεκτρολύτες και τους μη ηλεκτρολύτες
Όλες οι διαλυτές ουσίες αγώγουν ηλεκτρισμό
Η αγωγιμότητα εξαρτάται από το σχηματισμό ιόντων και όχι μόνο από τη διαλυτότητα.
Οι ισχυροί ηλεκτρολύτες είναι μόνο ισχυρά οξέα
Οι ισχυροί ηλεκτρολύτες περιλαμβάνουν επίσης ισχυρές βάσεις και διαλυτά άλατα.
Οι αδύναμοι ηλεκτρολύτες δεν μεταφέρουν ηλεκτρισμό
Αγωγούν, αλλά λιγότερο αποτελεσματικά επειδή παράγουν λιγότερα ιόντα.
Οι μη ηλεκτρολύτες δεν διαλύονται στο νερό
Πολλά διαλύονται, αλλά παραμένουν ως ουδέτερα μόρια.
Μη αγώγιμο σημαίνει αδιάλυτο
Μια ουσία μπορεί να διαλυθεί στο νερό και να μην άγει ηλεκτρισμό εάν δεν σχηματίζει ιόντα.
Συμπέρασμα
Η κύρια διαφορά μεταξύ ηλεκτρολυτών και μη ηλεκτρολυτών είναι ο σχηματισμός ιόντων.Αυτή η απλή ιδέα εξηγεί τον ρόλο τους στην αγωγιμότητα, τις αντιδράσεις και τις πρακτικές εφαρμογές.Μόλις το καταλάβετε, πολλές χημικές διεργασίες γίνονται πιο κατανοητές.
 Σχετικά με εμάς
Ικανοποίηση του πελάτη κάθε φορά.Αμοιβαία εμπιστοσύνη και κοινά συμφέροντα.
Σχετικά με εμάς
Ικανοποίηση του πελάτη κάθε φορά.Αμοιβαία εμπιστοσύνη και κοινά συμφέροντα.
δοκιμή λειτουργίας.Τα υψηλότερα οικονομικά αποδοτικά προϊόντα και η καλύτερη υπηρεσία είναι η αιώνια δέσμευσή μας.
Καυτό άρθρο
- LM358 Διπλός λειτουργικός ενισχυτής Περιεκτικός οδηγός: Pinouts, διαγράμματα κυκλώματος, ισοδύναμα, χρήσιμα παραδείγματα
- Είναι εναλλάξιμα τα CR2032 και CR2016;
- Κατανόηση των διαφορών ESP32 και ESP32-S3 Τεχνική και ανάλυση απόδοσης
- Επιλέγοντας τη σωστή μπαταρία: Οδηγός για τα AG4, LR626, LR66, 177/376/377, SR626 και SR626SW ισοδύναμα
- Βασικά στοιχεία τρανζίστορ BC547: Pinout, κυκλώματα εφαρμογής, εναλλακτικά/συμπληρωματικά μοντέλα
- NPN εναντίον PNP: Ποια είναι η διαφορά;
- ESP32 VS STM32: Ποιος μικροελεγκτής είναι καλύτερος για εσάς;
- Τι είναι το MOSFET και πώς λειτουργεί;
- Ηλεκτρικό ρελέ Basic: Λειτουργία εργασίας, τύποι και χρήσεις
- Τρανζίστορ PNP: δομή, αρχή εργασίας και εφαρμογή
 Alphanumeric Codes: How They Help Your Devices Work
Alphanumeric Codes: How They Help Your Devices Work
2026-04-29
 RS-232 έναντι RS-485: Ποιο είναι καλύτερο για το σύστημά σας
RS-232 έναντι RS-485: Ποιο είναι καλύτερο για το σύστημά σας
2026-04-29
Συχνές ερωτήσεις [FAQ]
1. Πώς επηρεάζει ο βαθμός διάστασης την ισχύ και την αγωγιμότητα του ηλεκτρολύτη;
Όσο περισσότερο μια ουσία διασπάται σε ιόντα, τόσο ισχυρότερο είναι ηλεκτρολύτη και όσο μεγαλύτερη είναι η αγωγιμότητά του.Η πλήρης διάσπαση παράγει πολλοί φορείς φορτίου, ενώ η μερική διάσταση περιορίζει τη ροή του ρεύματος.
2. Γιατί ένας ισχυρός ηλεκτρολύτης μπορεί να εξακολουθεί να παρουσιάζει χαμηλή αγωγιμότητα σε ορισμένες περιπτώσεις;
Εάν ένας ισχυρός ηλεκτρολύτης έχει χαμηλή διαλυτότητα, παράγει λιγότερα ιόντα λύση.Αυτό μειώνει την αγωγιμότητα παρόλο που διασπάται πλήρως.
3. Πώς επηρεάζει ο τύπος του χημικού δεσμού τη συμπεριφορά του ηλεκτρολύτη;
Οι ιοντικές και πολικές ομοιοπολικές ενώσεις τείνουν να σχηματίζουν ιόντα στο νερό, κάνοντας τους ηλεκτρολύτες.Οι μη πολικές ομοιοπολικές ενώσεις συνήθως παραμένουν ανέπαφες, άρα λειτουργούν ως μη ηλεκτρολύτες.
4. Πώς σχετίζεται η συμπεριφορά των ηλεκτρολυτών με τις αντιδράσεις οξέος-βάσης;
Οι ηλεκτρολύτες παρέχουν ιόντα όπως H+ και OH-, τα οποία οδηγούν την όξινη βάση αντιδράσεις.Η ισχύς του ηλεκτρολύτη επηρεάζει το πόσο πλήρως αυτά εμφανίζονται αντιδράσεις.
5. Πώς επηρεάζει η συγκέντρωση ιόντων τις ηλεκτροχημικές διεργασίες όπως οι μπαταρίες;
Η υψηλότερη συγκέντρωση ιόντων βελτιώνει τη μεταφορά φορτίου μεταξύ των ηλεκτροδίων, αύξηση της απόδοσης και της απόδοσης σε συσκευές όπως μπαταρίες και κυψέλες καυσίμου.
6. Πώς επηρεάζει τα βιολογικά συστήματα η ανισορροπία των ηλεκτρολυτών;
Η ανισορροπία μπορεί να διαταράξει τα νευρικά σήματα, τη μυϊκή σύσπαση και την καρδιά ρυθμό, που οδηγεί σε συμπτώματα όπως κόπωση, κράμπες ή πιο σοβαρή υγεία ζητήματα.
7. Γιατί είναι σημαντική η κατανόηση των ηλεκτρολυτών στις βιομηχανικές διεργασίες;
Οι ηλεκτρολύτες επιτρέπουν ελεγχόμενες χημικές αντιδράσεις, εξαγωγή μετάλλων, και την ηλεκτρόλυση, καθιστώντας τα σημαντικά στην κατασκευή και στα υλικά επεξεργασία.
Καυτός αριθμός εξαρτήματος
 CGJ5H4X7T2H223K115AA
CGJ5H4X7T2H223K115AA C1005JB0J475K050BC
C1005JB0J475K050BC CGJ4J2X7R0J474K125AA
CGJ4J2X7R0J474K125AA CL32B105KBHNNNF
CL32B105KBHNNNF 1206YC103JAT4A
1206YC103JAT4A TPSE226K035R0200
TPSE226K035R0200 TAP684K035CCS
TAP684K035CCS 0810-2H4R-28-F
0810-2H4R-28-F IXTN30N100L
IXTN30N100L MCP3425A1T-E/CH
MCP3425A1T-E/CH
- SP3077EEN-L
- CY7C65630-56LTXI
- MAX3491ECSD
- IDT71016S12PH
- EP4CE40F23A7N
- VE-J42-MW
- OARS1R010FLF
- SKKD380/22H4
- VI-253-CV/F2
- AD6620ASZ-REEL
- B88069X0720S102
- LP5900TLX-2.5/NOPB
- AD630ARZ-RL
- CR95HF-VMD5T
- TMS320DM8168BCYG2
- MSP430F5437AIPN
- TPS54614PWP
- 74HC4067D
- AD8610ARMZ
- IDT70V27L35PFI
- IP2022/PQ80-120U
- IP4770CZ16
- LB1638ML-TE
- LC5256MV-5F256-75I
- LTC3556EUFD
- MAX15034BAUI/V+T
- MAX713EWE
- OMAP2530BZAC
- PI74FCT541TQEX
- PS2861B-1-V-F3
- SST49LF002A-33-4C-NH
- TZA1024T/V2
- AZ8523-01B.R7G
- HX6512-A00DFAG-BAG
- IC42S32200-6T
- NT5DS64M8BS-5T
- RTD2673S-GR
- MC32PF3001A3
- XCS103VQG100C